Опыт лапароскопической илеоуретеропластики.
О.Э. Луцевич, Галлямов Эдуард Абдулхаевич, Н.Б. Забродина, К.С. Преснов, А.Б. Новиков, А.В. Коваленко, И.В. Мещанкин.
МГМСУ, кафедра факультетской хирургии №1; ЦКБ гражданской авиации, г. Москва.
Введение. Кишечная пластика – метод восстановления мочеточника при значительной протяженности дефекта, когда замещение за счет тканей мочевыводящих путей (лоханки, мочевого пузыря) невозможно. Идея данной операции высказана Finger в 1894 году. В 1900 году G. D'Urso и A. de Fabii выполнили её в эксперименте (на собаке). В 1940 году Nissen впервые выполнил тонококишечную пластику мочеточника у человека по поводу мочеточниково - кожного свища. Опыт лапароскопической кишечной пластики мочеточника в мире ограничен. В 2000 году Gill and colleagues произвели данную операцию. Использовались три порта, операционное время - 8 часов. В 2008 году Wagner et al. выполнили робот – ассистированную лапароскопическую кишечную пластику мочеточника за 9 часов.
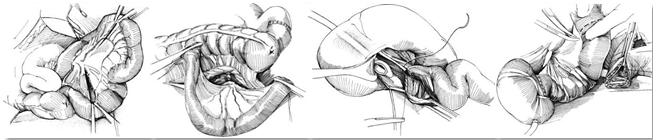
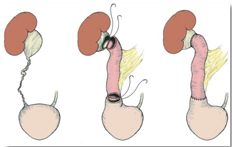
Рис. 1. Этапы и схематичный вид операции. Атлас Хинмана.
В России впервые данную операцию лапароскопическим доступом выполнил хирург И.Е. Хатьков в 2010 году; из урологов - А.Е. Санжаров (г. Екатеринбург) в 2011 году при ятрогенной травме мочеточника. Редкость патологии и сложность методики делают это вмешательство эксклюзивным, что и побудило нас поделиться собственным опытом.
Описание случая: Пациентка Р. 21 год. Диагностирован двусторонний гидронефроз, более выраженный слева. В 2012 году произведена лапароскопическая уретеропиелопластика слева по поводу стриктуры ЛМС, в ходе которой диагностирована еще и стриктура н/3 левого мочеточника. Симультанно выполнен лапароскопический уретероцистонеоанастомоз слева. В послеоперационном периоде возникла дисфункция стента, негерметичность уретеропиелоанастомоза, формирование забрюшинной уриномы, по поводу чего - ЧПНС слева. В дальнейшем, после удаления стента, рецидивировал гидронефроз слева. Этапное эндоскопическое лечение в течение 5 месяцев (бужирование мочеточника, рестентирование, уретеротомия (рис. 2)) успеха не принесло. Восстановить проходимость мочеточника, закрыть нефростому не удалось. Функциональная способность почки не изменена, суточный диурез 1,5 - 2 литра, удельный вес мочи 1010 - 1025.
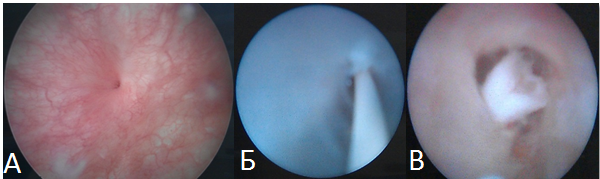
Рис. 2. Этап эндоскопического лечения.
А - цистоскопия, неоустье.
Б - стриктура мочеточника с проведенной через нее струной.
В - вид после уретеротомии
При обследовании, после очередного удаления стента, диагностирована протяженная облитерация н/3 мочеточника и рубцовый рестеноз лоханочно-мочеточникового сегмента (рис. 3), что потребовало полного замещения мочеточника.
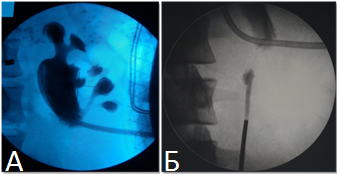
Рис. 3. Рестеноз лоханочно – мочеточникового сегмента.
А – антеградная пиелография.
Б – ретроградная пиелография.
Выполнена лапароскопическая илеоуретеропластика слева.
Хирургическая техника: Положение пациентки – «люмботомическое» на правом боку. Анестезия – эндотрахеальный наркоз. Карбоксиперитонеум - 12 мм.рт.ст. Установлено 5 троакаров: оптический - 10 мм параумбиликально слева. Инструментальные: 5 мм в левой подвздошной области, левом подреберье, по средней линии между пупком и лоном, и 10 мм правом подреберье по средне - ключичной линии. После рассечения брюшины по линии Тольди слева нисходящая ободочная и сигмовидная кишка смещены медиально. Обращает внимание выраженный рубцовый процесс в мезоколоне слева. Визуализированы почечные и брыжеечные сосуды слева, гонадная вена. Мобилизован мочеточник в верхней трети. Из–за резко выраженного забрюшинного рубцового процесса (ткани каменистой плотности), мобилизация лоханки проксимальнее ЛМС невозможна. Мочеточник иссечен от ЛМС до уровня перекреста с подвздошными сосудами (рис. 4, 5), представляет собой фиброзный склерозированный тяж с точечным просветом.
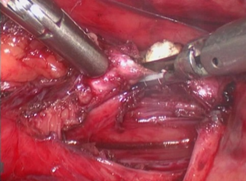
Рис. 4. Отсечение мочеточника от ЛМС.
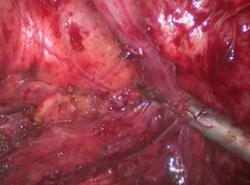
Рис. 5. Отсечение мочеточника в нижней трети.
Лоханка вскрыта при диссекции по просвету мочеточника (рис. 6).
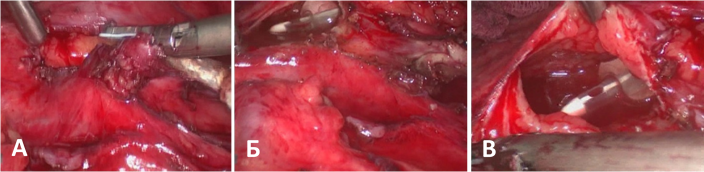
Рис. 6. А - Рассечение лоханки по просвету мочеточника.
Б, В - в лоханке виден баллон нефростомического дренажа
Мобилизован, изолирован на брыжейке аппаратным швом сегмент подвздошной кишки до 25 см длиной (рис.7).
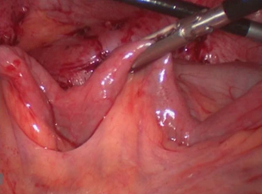
Рис. 7. Выбраный сегмент подвздошной кишки
Непрерывность кишечника восстановлена аппаратным илео-илео анастомозом "бок в бок" (рис. 8).
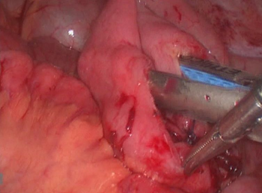
Рис. 8. Илео-илеоанастомоз
Сегмент подвздошной кишки проведен в забрюшинное пространство слева через окно брыжейки сигмовидной кишки (рис.9), размещен изоперистальтически позади нее.
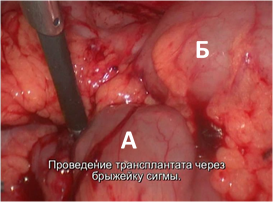
Рис. 9. Проведение кишечного трансплантата через брыжейку сигмы
А – трансплантат
Б – сигмовидная кишка
Проксимальный конец кишечного сегмента рассечен до 2 см по противобрыжеечному краю. Выполнен пиелоилеоанастомоз обивным швом (Полисорб 3.0) (рис.10).
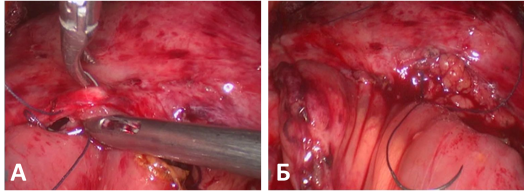
Рис. 10. Пиелоилеоанастомоз
А – ушивание анастомоза
Б – конечный вид
Проверка герметичности анастомоза при наполнении через нефростому: подтекания нет. Отсепарована брюшина от верхней и левой боковой стенок мочевого пузыря. В области верхушки произведена цистотомия до 2 см. К мочевому пузырю подведен дистальный конец кишечного сегмента, рассечен. Выполнен везикоилеоанастомоз двурядным швом (Полисорб 3.0) (рис.11).
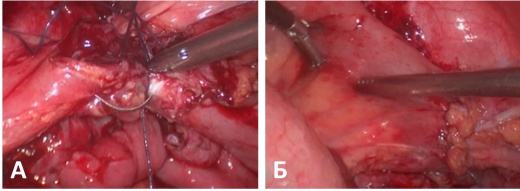
Рис. 11. Везикоилеоанастомоз
А – ушивание анастомоза
Б – конечный вид
При контрольном осмотре обращает на себя внимание «наполненность», раздутость трансплантата (рис. 12). Решено ретроградно установить дренаж – интубатор.
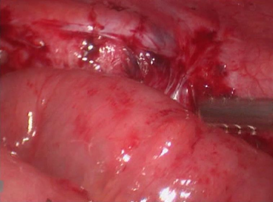
Рис. 12. Конечный вид кишечного трансплантата.
Выполнена цистоскопия. В "неоустье" беспрепятственно введен цистоскоп. Везикоилеоанастомоз свободно проходим, герметичен (рис. 13). Слизистая кишки розового цвета. Под двойным видеоконтролем (лапаро- и цистоскопическим) ретроградно по струне-проводнику в кишечный сегмент установлен дренаж – интубатор (рис. 14), выведен через уретру, фиксирован на катетере Фолея. Установлены дренажи. Раны ушиты. Операция завершена.
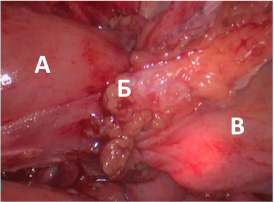
Рис. 13. Цистоскопия.
А - кишечный трансплантат
Б - илеовезикоанастомоз
В - мочевой пузырь
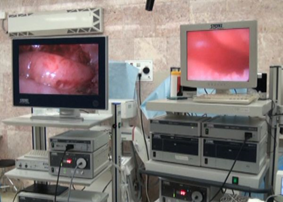
Рис. 14. Дренирование трансплантата под двойным видеоэндоскопическим контролем. Вид операционной
Результаты. Длительность операции составила 240 мин. Кровопотеря - 150 мл. Интра- и послеоперационных осложнений не было. Дренажи из брюшной полости удалены на 2 - 4 сутки; дренаж из кишечного трансплантата - на 15 сутки, нефростома - на 17 сутки. Нефростомический свищ закрылся. При контрольном УЗИ нарушений уродинамики не выявлено. Послеоперационный койко-день – 20.
Морфологическое заключение: макро: фрагмент мочеточника длиной 5 см диаметром 0,5 - 0,7 см (рис. 15). Микро: в гистопрепаратах фрагменты мочеточника со звездчатым и щелевидным просветом, явлениями хронического воспаления. Отмечается утолщение стенки мочеточника за счет неравномерной гипертрофии мышечного слоя и фиброза.
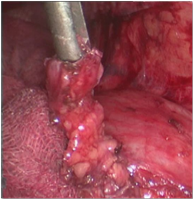
Рис. 15. Удаленный фрагмент мочеточника.
Заключение. Реконструктивно–пластические вмешательства в урологии являются одними из самых сложных, требуют высокого хирургического мастерства, слаженной работы операционной бригады, адекватной технической оснащенности. В ходе выполнения представленной операции, зона хирургического интереса обширна, манипуляции проведенысь в различных анатомических зонах (забрюшинное пространство, брюшная полость, малый таз), что потребовало большого опыта, мультидисциплинарного подхода (урология, абдоминальная хирургия, гинекология). Использование современных технологий (ультразвуковая, биполярная энергии, сшивающие аппараты) упрощают вмешательство, делая его более безопасным и сокращая операционное время. Тем не менее, хорошее владение интракорпоральным лапароскопическим швом является не желаемой опцией для хирурга, а одним из основных требований. При соблюдении всех условий, лапароскопическая методика столь сложного вмешательства является выполнимой, безопасной для пациента, позволяет произвести операцию в полном объеме, без ограничений возможности доступа, сохраняя при этом все преимущества малоинвазивной хирургии, с хорошим функциональным эффектом и ранней реабилитацией пациентов.
